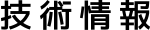金属によっては、【図1】に示した金属の活性化系列(イオン化傾向)の列から判断されるよりは、はるかに化学的安定性の高いものがあります。アルミニウム、ニッケル、チタン、クロム、モリブデンなどであります。これらの金属は決して系列の貴側にあるわけではありません。チタンはマグネシウムとアルミニウムの間あたり、クロム、モリブデンは鉄よりやや上位にあると考えられます。
これらの金属が化学的に安定な訳は、表面に「不動態皮膜」と呼ばれる皮膜を形成し易いからであります。不動態皮膜は一種の酸化物でありますが、数ナノメータと非常に薄くて透明で目には見えません。したがって、不動態皮膜が形成された後も、元の金属光沢を保っています。またこの皮膜は、環境に触れた途端に瞬間的に形成されます。もちろん時間が経てば成長してより安定になりますが、薄膜でも化学的安定性を直ちに有することが特徴です。不動態皮膜を持つようになることを「不動態化」といい、不動態皮膜をもっている状態を「不動態」といいます。
不動態皮膜をもつことの最大の特徴は、腐食がほぼゼロになることです。もう一つの特徴は、金属の活性系列(イオン化傾向)の位置に見合う挙動をせず、ずっと貴の方向にあるかのように振る舞うことです。
異なった金属を接触させて海水中に浸漬すると、一方がプラス極、他方がマイナス極となって、マイナス極のほうが腐食します。よりプラス極になりやすい性質を貴(き)、マイナス極になりやすい性質を卑(ひ)といいます。クロム、チタンなど不動態皮膜を作りやすい金属は、不動態皮膜を生成することによって、皮膜のないときに比べ、ずっと「貴」な性質をもつようになります。
不動態皮膜を作るのは、先に述べた限られた金属と、それらの金属を主成分として含む合金だけです。しかしこれらの金属や合金も、不動態皮膜ができるかどうかは、環境条件に依存します。
これらの金属のほとんどは、溶存酸素を含む中性の水中で不動態化します。塩酸や希硫酸などの非酸化性の酸の中では、酸の濃度がごく低いときには不動態化しますが、濃度が濃くなると不動態皮膜が溶けてしまいます。このような状態を「活性態」といいます。
硝酸のように酸化性の酸の中では、不動態皮膜は原則的に安定です。アルカリ性溶液でも安定です。濃硝酸や濃硫酸のように酸化力の強い酸の中では、鉄も容易に不動態化します。
ステンレス鋼は多量のクロムを含むため、容易に不動態化する合金です。ステンレス鋼が溶存酸素を含む中性の水中にあるとき、不動態皮膜によって守られていますが、海水のように塩素イオンがリッチな水中では例外です。塩素イオンは、不動態皮膜を局部的に破壊し、その小さい部分の深い孔食を生じさせます。